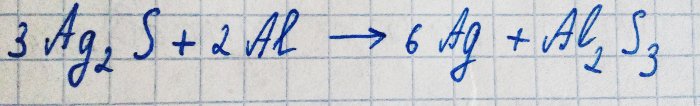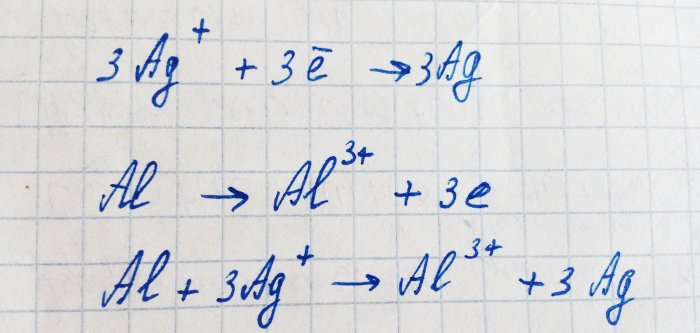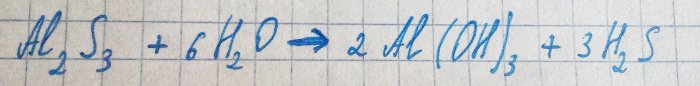Limpiar artículos de plata en casa.
Recientemente me encontré con un juego de cubiertos de plata que tiene unos cien años. Durante este tiempo, las cucharas y cuchillos lograron oscurecerse y oxidarse, y decidí limpiarlos de los depósitos que se habían formado. En este artículo, compartiré una forma bastante eficaz de restaurar sus cubiertos antiguos a su brillo original. Entonces vamos.
Teoría
Primero, averigüemos por qué la plata se oscurece con el tiempo y de dónde proviene el óxido.
La plata (Ag) prácticamente no muestra reactividad con el oxígeno o el agua, es decir, no se oxida. Esta propiedad fue notada por primera vez por los alquimistas; comenzaron a llamar a la plata un metal noble.
Sin embargo, la plata reacciona con el sulfuro de hidrógeno en presencia de oxígeno. La ecuación para esta reacción es la siguiente:
El sulfuro de plata resultante simplemente cubre el metal con una película oscura, evitando una mayor oxidación.
Si los cubiertos no están hechos de plata pura (por ejemplo, estándar 800), las impurezas de la aleación se oxidan.
Eliminación de óxido
Prepare una solución de ácido cítrico. Cuanto más saturado esté, más rápida y violenta será la reacción.Le ponemos los cubiertos, cuando dejan de salir burbujas de gas, las sacamos de la solución, enjuagamos con agua y limpiamos con una toalla de papel.
Para obtener mejores resultados, puedes calentar la solución a 80°C, pero es importante seguir las precauciones de seguridad.
eliminación de placa
Para eliminar la placa, utilizaremos el método químico de reducir el sulfuro de plata a metal libre.
Para esto necesitamos:
- - el recipiente donde tendrá lugar la reacción;
- - bicarbonato de sodio;
- - papel de aluminio;
- - sal de mesa;
- - agua caliente.
Coloque papel de aluminio en el fondo del recipiente y objetos plateados encima, con el lado oscuro hacia abajo.
Espolvorea refresco encima.
Ahora disuelve la sal en agua a razón de 6 cucharadas por litro de agua. Vierta la solución resultante en el recipiente, comienza una reacción con la liberación de sulfuro de hidrógeno y dióxido de carbono.
Todo el proceso debe realizarse al aire libre, porque el sulfuro de hidrógeno tiene un olor característico a huevos podridos y es perjudicial para la salud.
Veamos la química de lo que está sucediendo.
Primero, la soda disuelve la fina película de hidróxido de la superficie del papel de aluminio.
Esto le da al sulfuro de plata la oportunidad de reaccionar directamente con el aluminio.
El aluminio tiene una energía de ionización menor que la plata. Se oxida a un ion, dándole a la plata sus electrones. Este proceso se puede escribir así:
Esta reacción es electroquímica: debido al movimiento de electrones del aluminio a la plata, aparece una diferencia de potencial.
La sal en una solución mejora su conductividad, permitiendo que la reacción se complete.
El sulfuro de aluminio liberado reacciona inmediatamente con el agua:
De ahí el sulfuro de hidrógeno y el olor correspondiente.
Este proceso puede tardar hasta media hora. Cuando termine, enjuague los cubiertos con agua y séquelos con una toalla.
Después de la restauración de la plata, puedes utilizar medios especiales para conservarla. Protegen la superficie plateada de la humedad y el sulfuro de hidrógeno.
De esta forma la plata conservará su brillo durante mucho tiempo.
Conclusión
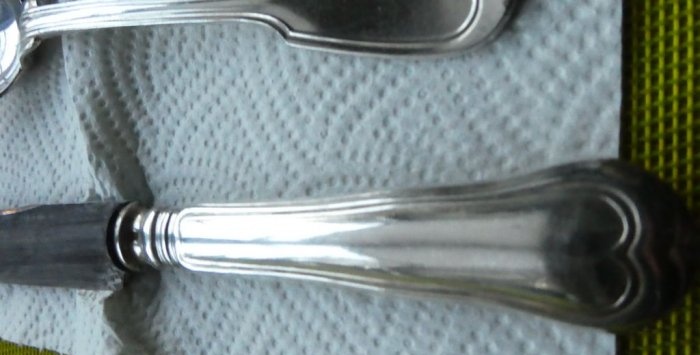
Fotos de platos restaurados:
Como puede ver, no hay rastro de oscurecimiento en las cucharas. Los cuchillos también empezaron a tener mejor aspecto, pero lamentablemente parte de la capa de plata desapareció de su superficie y el tiempo todavía pasa factura. Tendrás que llevarlos a un especialista para que los vuelva a platear.
Y este artículo ha llegado a su fin. ¡Buena suerte con vuestra repetición a todos!
Artículo original en inglés.
Clases magistrales similares
Particularmente interesante
Comentarios (0)