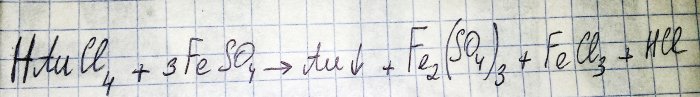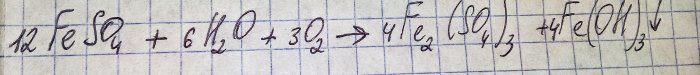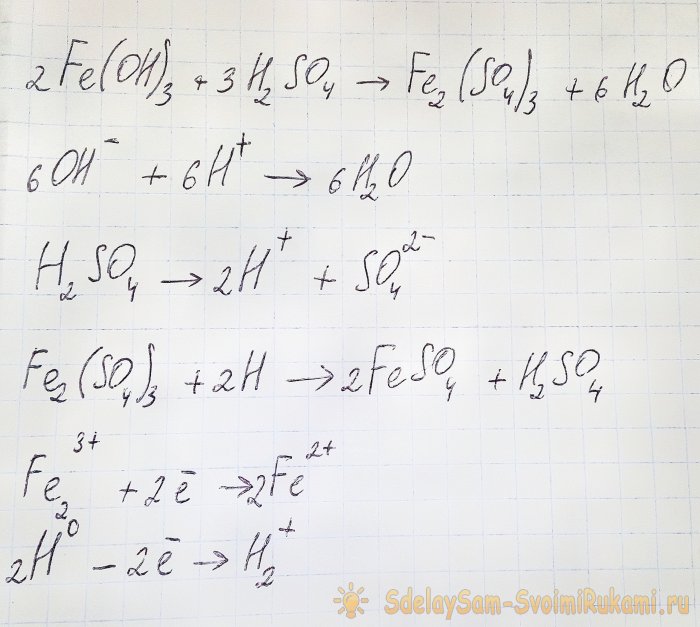Brz način dobivanja željeznog sulfata iz gnojiva
Pretposljednji korak na putu dobivanja plemenitog metala iz radio komponenti je redukcija potonjeg iz odgovarajućeg klorida. Željezo(II) sulfat je odličan za ove namjene. Razmotrite jednadžbu za ovu reakciju:
HAuCl4 - vodikov tetrakloroaurat (III) - spoj koji nastaje otapanjem zlata u carskoj vodici. Za sada nećemo ulaziti dublje u ovaj proces jer zaslužuje poseban članak.
Dakle, sulfat (u daljnjem tekstu se misli na željezo(II) sulfat) je jedan od jeftinih i lako dostupnih redukcijskih sredstava. U trgovinama se može naći pod nazivom "željezni sulfat", to je gnojivo. Ali ovo nije čista tvar, udio sulfata u njemu je oko 50%, ostatak su nečistoće. I prije nego što možemo obnoviti zlato, moramo pročistiti naš sulfat.
Trebat će
Za ovo će vam trebati:
- Željezni sulfat (prodaje se u dućanima kao “sve za vrt”, kupila sam kilogram da mi bude za glavu);
- Otopina sumporne kiseline, također poznata kao kiseli elektrolit za akumulatore (u salonima automobila);
- Alkohol, koristio sam 95%;
- Kemijski ili jednokratni pribor (šalice, žlice za miješanje).
Željezni sulfat dobivamo iz gnojiva
Za pripremu otopine koristim staklenu posudu. Unutra je 500 ml vruće vode, možda malo manje.
Sada izmjerite otprilike pola čaše gnojiva:
Kao što vidite, tvar je žuto-smeđe boje; takav prljavi "sulfat" može se koristiti samo za namjeravanu svrhu - za prskanje vegetacije. Imamo druge ciljeve.
Ulijte u staklenku:
Otopina je poprimila neugodnu smeđu boju. Do bojanja je došlo zbog reakcije gnojiva s vodom:
Željezo u sulfatu oksidira se u trovalentno, a taloži se željezov(III) hidroksid, što je zapravo i razlog njegove boje.
Da bi se iz dobivenih spojeva dobio sulfat koji nas zanima, potrebno je otopinu zakiseliti sumpornom kiselinom. Dodajte u malim obrocima dok otopina ne posvijetli.
U tom slučaju dolazi do sljedećih reakcija:
Hidroksid reagira s kiselinom pri čemu nastaje željezov(III) sulfat (reakcija ionske izmjene). On zauzvrat reagira s atomskim vodikom, koji nastaje tijekom disocijacije sumporne kiseline. Posljednja reakcija je redoks.
Sada otopina sadrži upravo onoliko sulfata koliko nam je potrebno, ali je sama otopina još uvijek mutna. Pustite da odstoji i filtrirajte, koristio sam kemijski filter.
Na dnu posude ostale su netopljive nečistoće:
Isperemo ga i u njega ulijemo procijeđenu otopinu. Mnogo je lakši i čišći od originala.
Etilni alkohol istiskuje soli dibazičnih kiselina iz njihovih otopina. To ćemo svojstvo iskoristiti za dobivanje krutog sulfata. U otopinu dodamo alkohol, ulio sam 200 ml, što je po volumenu jednako nešto više od polovine izvornog volumena gnojiva.
Na dnu su se pojavili kristali našeg sulfata.
Otopinu sam ostavio dva dana tako da je sav sulfat imao vremena da se istaloži.
U početku možete dodati više alkohola kako bi ovaj proces bio brži.
Ocijedite tekućinu, lupkajući po dnu i blagim zagrijavanjem, odvojite sulfat od staklenke i izlijte ga na papirnati ručnik da se osuši.
Nakon nekoliko sati, ulijte sulfat u staklenu posudu, označite tvar iu ovom obliku može se pohraniti dugo vremena.
Budući da su se kristalni hidrati istaložili, formula tvari je kao na slici. Ali to nas ne sprječava da ga koristimo za vlastite potrebe, svejedno ga otopimo u vodi.
Zaključak
Sigurnosne mjere opreza i poštivanje pravila za rukovanje kiselinama su dani. Ni u kojem slučaju ne smijemo zaboraviti na njih.
Čiste tvari za sve!
Slične majstorske tečajeve
Posebno zanimljivo
Komentari (1)