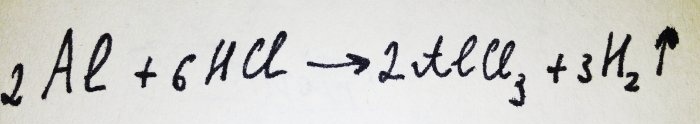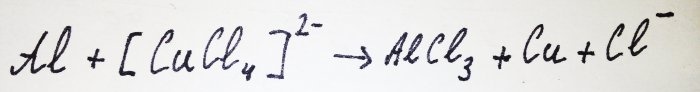Paprastas eksperimentas – Mėlyna liepsna
Laba diena, smalsūs chemikai! Šiandien atliksime paprastą, bet įspūdingą eksperimentą.
Jo esmė ta, kad reakcijos metu išsiskiriantis vandenilis dega mėlyna liepsna.
Taigi, mums reikės:
Eksperimentą atliksime stikliniame inde.
Kaip indą galite naudoti Petri lėkštelę arba stiklinę. Nerekomenduoju naudoti kolbos, nes deguonies srautas viduje bus sunkus dėl siauro kolbos kaklelio.
Prieš atliekant šį eksperimentą, primygtinai rekomenduoju susipažinti su saugos priemonėmis dirbant su rūgštimis.
Į stiklainį supilkite arbatinį šaukštelį vitriolio ir įpilkite 40 ml rūgšties. Tirpalas tampa žalias, nes susidaro kompleksinis vario jonų tetrachlorokupratas [CuCl4]2-.
Dabar belieka pridėti aliuminio foliją. Jis yra padengtas oksido plėvele, tačiau susidaręs kompleksas greitai ją sunaikina. Tada dalis aliuminio reaguoja su rūgštimi, šios reakcijos lygtis yra tokia:
Kaip matyti iš reakcijos, išsiskiria vandenilis.
Likusi aliuminio dalis sąveikauja su kompleksu, išstumdama iš jo varį:
Reakcijos vyksta greitai, išsiskiria daug šilumos.
Išsiskyręs vandenilis gerai dega ore, padegkime.
Siauras liepsnos srautas siejamas su stiklainio kaklelio savybėmis, o sodrią mėlyną spalvą jam suteikia tirpale esantys vario jonai.
Atlikime tą patį eksperimentą, bet kitame konteineryje:
Kai visas aliuminis sureaguoja, tirpalas tampa pilkas, o paviršiuje yra redukuoto vario dėmės. Jį reikia atskiesti dideliu kiekiu vandens ir išpilti į kanalizaciją.
Dugne liko nuosėdų:
Taip pat turėtumėte jo atsikratyti, nes pabandžius filtruoti ant filtro liko šviesiai rudos nuosėdos, kurių negalima pavadinti variu.
Ir tuo šis straipsnis baigiamas. Šią patirtį galima pademonstruoti per chemijos pamokas mokykloje. Sėkmės visiems kartojant!
Jo esmė ta, kad reakcijos metu išsiskiriantis vandenilis dega mėlyna liepsna.
Reagentai
Taigi, mums reikės:
- Druskos rūgšties koncentracija 15%;
- vario sulfatas;
- Aliuminio folija.
Eksperimentą atliksime stikliniame inde.
Kaip indą galite naudoti Petri lėkštelę arba stiklinę. Nerekomenduoju naudoti kolbos, nes deguonies srautas viduje bus sunkus dėl siauro kolbos kaklelio.
Eksperimentuokite
Prieš atliekant šį eksperimentą, primygtinai rekomenduoju susipažinti su saugos priemonėmis dirbant su rūgštimis.
Į stiklainį supilkite arbatinį šaukštelį vitriolio ir įpilkite 40 ml rūgšties. Tirpalas tampa žalias, nes susidaro kompleksinis vario jonų tetrachlorokupratas [CuCl4]2-.
Dabar belieka pridėti aliuminio foliją. Jis yra padengtas oksido plėvele, tačiau susidaręs kompleksas greitai ją sunaikina. Tada dalis aliuminio reaguoja su rūgštimi, šios reakcijos lygtis yra tokia:
Kaip matyti iš reakcijos, išsiskiria vandenilis.
Likusi aliuminio dalis sąveikauja su kompleksu, išstumdama iš jo varį:
Reakcijos vyksta greitai, išsiskiria daug šilumos.
Išsiskyręs vandenilis gerai dega ore, padegkime.
Siauras liepsnos srautas siejamas su stiklainio kaklelio savybėmis, o sodrią mėlyną spalvą jam suteikia tirpale esantys vario jonai.
Atlikime tą patį eksperimentą, bet kitame konteineryje:
Kai visas aliuminis sureaguoja, tirpalas tampa pilkas, o paviršiuje yra redukuoto vario dėmės. Jį reikia atskiesti dideliu kiekiu vandens ir išpilti į kanalizaciją.
Dugne liko nuosėdų:
Taip pat turėtumėte jo atsikratyti, nes pabandžius filtruoti ant filtro liko šviesiai rudos nuosėdos, kurių negalima pavadinti variu.
Išvada
Ir tuo šis straipsnis baigiamas. Šią patirtį galima pademonstruoti per chemijos pamokas mokykloje. Sėkmės visiems kartojant!
Panašios meistriškumo klasės
Ypatingai įdomu
Komentarai (2)