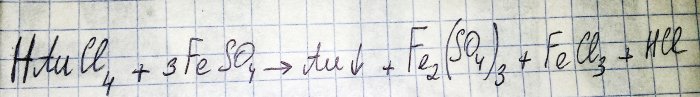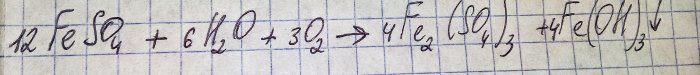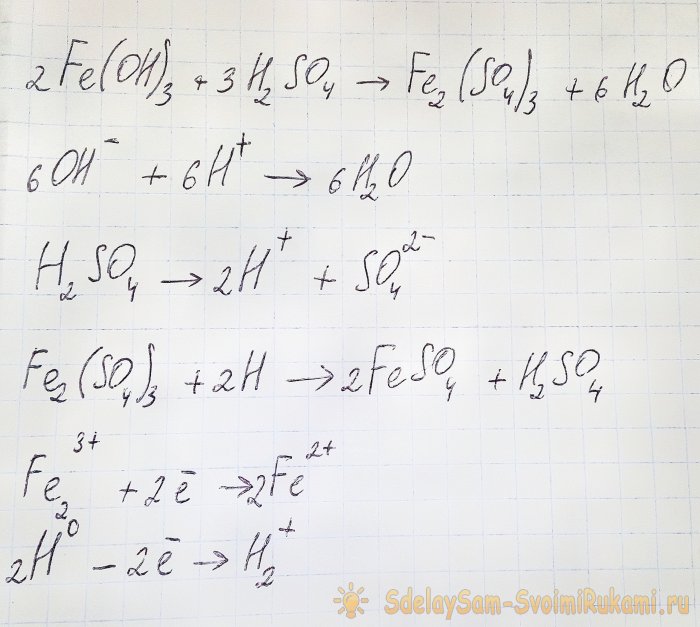Greitas būdas gauti geležies sulfatą iš trąšų
Priešpaskutinis žingsnis kelyje į tauriojo metalo gavimą iš radijo komponentų yra pastarųjų redukavimas iš atitinkamo chlorido. Šiems tikslams puikiai tinka geležies (II) sulfatas. Apsvarstykite šios reakcijos lygtį:
HAuCl4 – vandenilio tetrachloroauratas (III) – junginys, kuris susidaro ištirpus auksui regio vandenyje. Į šį procesą kol kas nesigilinsime, nes jis nusipelno atskiro straipsnio.
Taigi sulfatas (toliau – geležies(II) sulfatas) yra vienas pigiausių ir lengvai prieinamų reduktorių. Parduotuvėse jį galima rasti pavadinimu „geležies sulfatas“, tai yra trąša. Bet tai nėra gryna medžiaga, sulfato dalis joje yra apie 50%, likusi dalis yra priemaišos. Ir prieš atkurdami auksą, turime išvalyti sulfatą.
Reikės
Tam jums reikės:
- Geležies sulfatas (parduotuvėse parduodamas kaip „viskas daržui“; pirkau kilogramą, kad užtektų galvai);
- Sieros rūgšties tirpalas, taip pat žinomas kaip rūgštinis elektrolitas akumuliatoriams (automobilių salonuose);
- Alkoholis, naudojau 95%;
- Cheminiai arba vienkartiniai indai (puodeliai, maišymo šaukštai).
Geležies sulfatą gauname iš trąšų
Tirpalui ruošti naudoju stiklinį indelį. Viduje yra 500 ml karšto vandens, gal kiek mažiau.
Dabar išmatuokite apie pusę stiklinės trąšų:
Kaip matote, medžiaga yra geltonai rudos spalvos, toks nešvarus „sulfatas“ gali būti naudojamas tik pagal paskirtį - purkšti augmeniją. Turime kitų tikslų.
Supilkite jį į stiklainį:
Tirpalas tapo nemalonios rudos spalvos. Dažymas atsirado dėl trąšų reakcijos su vandeniu:
Geležis sulfate oksiduojasi iki trivalentės, o geležies (III) hidroksidas nusėda, o tai iš tikrųjų yra jo spalvos priežastis.
Norint iš gautų junginių gauti mus dominantį sulfatą, tirpalą reikia parūgštinti sieros rūgštimi. Įpilkite mažomis porcijomis, kol tirpalas pašviesės.
Tokiu atveju pasireiškia šios reakcijos:
Hidroksidas reaguoja su rūgštimi, sudarydamas geležies (III) sulfatą (jonų mainų reakcija). Savo ruožtu jis reaguoja su atominiu vandeniliu, kuris susidaro disociuojant sieros rūgštį. Paskutinė reakcija yra redoksas.
Dabar tirpale yra būtent toks sulfatas, kurio mums reikia, tačiau pats tirpalas vis dar drumstas. Leiskite sėdėti ir filtruokite, aš naudojau cheminį filtrą.
Stiklainio apačioje liko netirpių priemaišų:
Nuplauname ir supilame filtruotą tirpalą. Jis yra daug lengvesnis ir švaresnis nei originalas.
Etilo alkoholis išstumia dvibazių rūgščių druskas iš jų tirpalų. Šią savybę panaudosime kietajam sulfatui gauti. Į tirpalą įpilame spirito, aš įpyliau 200 ml, tai tūriu prilygsta kiek daugiau nei pusei pradinio trąšų tūrio.
Apačioje pasirodė mūsų sulfato kristalai.
Palikau tirpalą dvi dienas, kad visas sulfatas spėtų nusodinti.
Iš pradžių galite pridėti daugiau alkoholio, kad šis procesas būtų greitesnis.
Nusausinkite skystį, bakstelėdami dugną ir švelniai kaitindami, atskirkite sulfatą nuo stiklainio ir supilkite ant popierinio rankšluosčio, kad išdžiūtų.
Po kelių valandų supilkite sulfatą į stiklinį indelį, pažymėkite medžiagą ir tokioje formoje ją galima ilgai laikyti.
Kadangi iškrito kristaliniai hidratai, medžiagos formulė yra tokia, kaip parodyta paveikslėlyje. Bet tai netrukdo mums jo naudoti savo reikmėms, bet kokiu atveju ištirpinti vandenyje.
Išvada
Saugos priemonės ir rūgščių tvarkymo taisyklių laikymasis yra duota. Jokiu būdu neturėtume jų pamiršti.
Švarios medžiagos visiems!
Panašios meistriškumo klasės
Ypatingai įdomu
Komentarai (1)