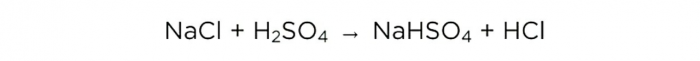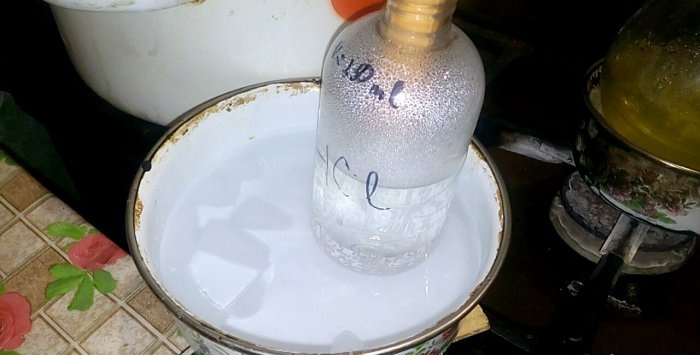Прављење хлороводоничне киселине код куће
Алхемичари који су први произвели хлороводоничну киселину у 15. веку назвали су је „спиритус салис“, „дух из соли“. У то време ова киселина је имала магична својства: кородирала је папир, растварала метале, тровала људе. Ова својства остају са њим до данас, али сада је ова киселина довољно проучена, и ту нема магије.
Хлороводонична киселина (ХЦл) је јака једнобазна киселина, у свом чистом облику је провидна течност. У својој максималној концентрацији од 38% „дими“ се у ваздуху. Добићемо киселину са концентрацијом од половине мање.
Па хајде да почнемо.
Мере безбедности
Будите опрезни када радите са токсичним супстанцама!
Сви експерименти се морају изводити у добро проветреној просторији или испод хаубе. Обавезно носите заштитне наочаре (могу се купити у продавници гвожђара) и рукавице (ако не можете да пронађете специјалне хемијске рукавице, погодне су оне доброг квалитета за прање судова).
Сода бикарбона мора бити присутна на месту експеримента како би се неутралисала киселина у непредвиђеној ситуацији (ово ће ослободити угљен-диоксид и воду).
Строго је забрањено извођење експеримената у металним посудама.
Требаће
За спровођење експеримента биће нам потребно:
- Кисели електролит за батерије (продаје се у продавници аутомобила);
- дестилована вода (ибид);
- Столна со (доступна у свакој кухињи);
- Сода бикарбона (погледајте мере предострожности).
Од посуђа вам је потребно:
- Стаклена боца;
- Посуда са песком у коју можете ставити боцу;
- Неколико чаша за једнократну употребу 200 мл;
Ако имате боцу отпорну на топлоту, можете је загрејати под отвореним пламеном горионика. Али ипак препоручујем коришћење песка, у том случају ће апсорбовати киселину.
Такође ће вам требати пар водоводних углова пречника 50 мм и горионик (у мом случају алкохол, али препоручујем коришћење гасног).
Фаза 1 - испаравање
Електролит за батерије је 36% сумпорне киселине (Х2СО4). Прво морамо повећати његову концентрацију.
У чашу, односно скоро до ивице, сипајте 200 мл и у боцу сипајте нешто више од половине стакла. Означите маркером и додајте остатак.
Око боце сам поставио рефлектор од фолије ради ефикаснијег загревања, али сам га касније уклонио јер је почео да се топи.
Сада ставите посуду на горионик и испарите до нивоа претходно постављене ознаке, чак и мало ниже.
Истовремено, на угао стављамо неколико пута пресавијену газу и причврстимо је еластичном траком. Припремите незасићени раствор соде и уроните у њега крај угла са газом.
Када електролит почне да кључа, стављамо угао на тиквицу, чврсто седи на њему. Крај газе усмеравамо у отворени прозор.
Ово је неопходно ако изненада сама сумпорна киселина почне да испарава заједно са водом. Ако не прегрејете боцу превише, то се неће догодити.
Горионик у акцији:
Мој горионик је релативно мале снаге, тако да је испаравање трајало око сат времена.Гасни горионик или електрични шпорет би значајно убрзао овај процес.
Након завршетка прве фазе, у боци треба да остане нешто мање од половине раствора, односно киселине са концентрацијом од око 75%. Не заборавите на тачност.
Оставите да се охлади на собној температури.
Фаза 2 - прорачуни
Сада када имамо концентровану сумпорну киселину, можемо да изведемо основну реакцију, она изгледа овако:
Али прво, хајде да направимо неке прорачуне, а на крају ћемо их упоредити са оним што се догодило у пракси.
Дакле, у почетку смо имали 200 мл електролита са густином од 1,27 г/цм³. Гледајући табелу густина сумпорне киселине, видимо да ова густина одговара концентрацији од 36%. Израчунајмо запремину киселине:
200мл*36%=72мл - В(Х2СО4)
Након што смо испарили раствор, његова концентрација, а самим тим и густина, се повећала. Гледамо исту табелу и видимо да концентрација од 75% одговара густини од 1,67 г/цм³.
Знајући густину струје (п) и запремину (В) киселине, сазнајемо масу:
м=п*В;
м(Х2СО4)=1,67 г/цм³ * 72мл=120г;
м(Х2СО4)=1,67 г/цм³ * 72мл=120г;
Сада се сећамо из школске хемије:
м(Х2СО4)/М(Х2СО4)=м(НаЦл)/М(НаЦл)=м(ХЦл)/М(ХЦл),
где је М моларна маса супстанце.
где је М моларна маса супстанце.
Моларне масе Х2СО4, НаЦл и ХЦл су 98, 58,5 и 36,5 г/мол, респективно. Сада можемо да сазнамо колико је кухињске соли потребно и колико ћемо ХЦл добити.
Наиме, потребно нам је 72 г НаЦл, то је 34 мл, узмимо га у вишку - четвртина чаше.
Одлично, а ХЦл у теорији ће изаћи на 44,7 г.
Табела густине ХЦл има колону г/л. Одатле узимамо вредност за концентрацију од 15% - 166,4 г/л. Запремина воде потребна за добијање 15% ХЦл је 44,7/166,4≈270мл. Узећемо 200 мл. Као резултат, у теорији ћу добити 22% хлороводоничне киселине.
Фаза 3 - добијање киселине
Повезујемо два угла на следећи начин:
А цела структура ће изгледати овако:
Одговарајућа киселина ће се кондензовати у посуду са ознаком ХЦл; запремина воде у њој је 200 мл. Такође означите тренутни ниво течности на овој посуди.
Уклонимо углове и сипамо израчунату количину соли у тиквицу кроз левак.
Решење постаје жуто.
Да би хлороводонична киселина почела да се ослобађа, потребно је да укључите горионик. Али прво, чврсто причврстимо углове на тиквицу и посуду за пријем.
Када се киселина кондензује у води, формирају се "вертикални таласи". Такође, раствор се загрева и мора се охладити. На пример, испод можете поставити другу посуду са ледом.
Реакција се одвија релативно брзо - 20 минута, након чега можете искључити топлоту. Пустите да се последње паре хлороводоничне киселине растворе у води, а затим херметички затворите посуду. Када се боца охлади, преостали раствор разблажите водом (отприлике један према један) и сипајте у канализацију.
Суштина
Ознаком на посуди одређујемо колико је течности додато. За мене је то ⅙, односно 17%. Ово је концентрација наше хлороводоничне киселине. Хајде да га упоредимо са оним добијеним у теорији.
17%/22%*100%=77% - принос реакције.
Важно је напоменути да не постоји излаз једнак 1, увек постоје губици. У мом случају, ово је недовољно испарен електролит. У идеалном случају, концентрација сумпорне киселине треба да буде 90-95%.
Хајде да проверимо резултујућу киселину за интеракцију са металом.
Уочавамо брзу еволуцију водоника. То значи да је киселина погодна за даље експерименте.
Варијације
Као тиквицу можете користити чисту стаклену флашу пива или соде, али под условом да је загревање што је могуће глатко. Уместо ПВЦ углова, можете узети полипропиленске цеви и углове мањег пречника (погодно за вашу боцу).
Још једном вас позивам да поштујете мере предострожности. Срећна искуства свима!
Сличне мајсторске класе
Посебно занимљиво
Коментари (19)