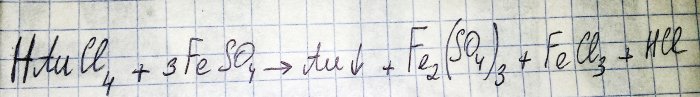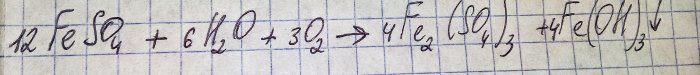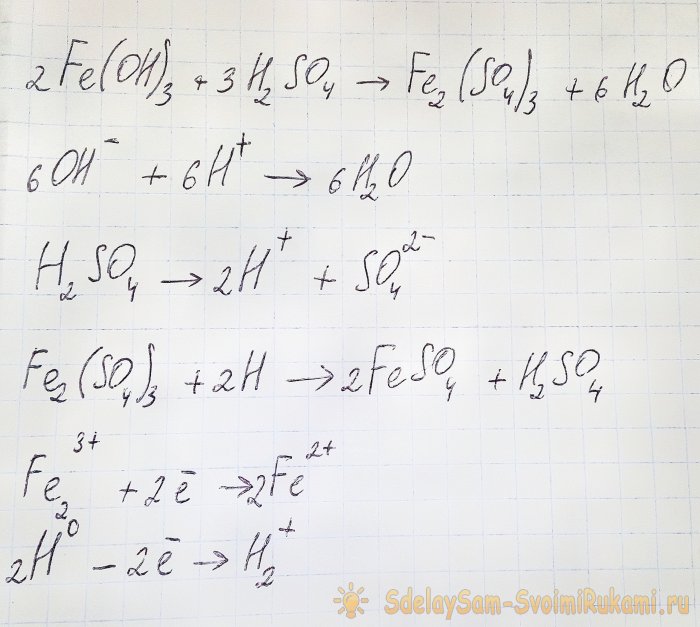Брз начин за добијање жељезног сулфата из ђубрива
Претпоследњи корак на путу ка добијању племенитог метала од радио компоненти је редукција последњег из одговарајућег хлорида. Гвожђе(ИИ) сулфат је одличан за ове сврхе. Размотрите једначину за ову реакцију:
ХАуЦл4 - водоник тетрахлороаурат (ИИИ) - једињење које настаје када се злато раствори у царској водици. За сада нећемо улазити дубље у овај процес, јер заслужује посебан чланак.
Дакле, сулфат (у даљем тексту се мисли на гвожђе(ИИ) сулфат) је један од јефтиних и лако доступних редукционих агенаса. У продавницама се може наћи под називом „гвоздени сулфат“, то је ђубриво. Али ово није чиста супстанца, удео сулфата у њему је око 50%, остало су нечистоће. И пре него што можемо да обновимо злато, морамо да прочистимо наш сулфат.
Требаће
За ово ће вам требати:
- Гвоздени сулфат (продаје се у продавницама типа „све за башту“; купио сам килограм да ми буде довољно за главу);
- Раствор сумпорне киселине, познат и као кисели електролит за акумулаторе (у ауто кућама);
- Алкохол, користио сам 95%;
- Хемијски или једнократни прибор за јело (шоље, кашике за мешање).
Добијамо гвожђе сулфат из ђубрива
За припрему раствора користим стаклену теглу. Унутра има 500 мл вреле воде, можда мало мање.
Сада измерите око пола чаше ђубрива:
Као што видите, супстанца је жуто-браон боје; такав прљави "сулфат" може се користити само за његову намену - за прскање вегетације. Имамо друге циљеве.
Сипајте у теглу:
Раствор је добио непријатну браон боју. До бојења је дошло услед реакције ђубрива са водом:
Гвожђе у сулфату се оксидира до тровалентног, а гвожђе(ИИИ) хидроксид преципитира, што је заправо разлог његове боје.
Да бисмо од добијених једињења добили сулфат који нас занима, потребно је закиселити раствор сумпорном киселином. Додајте у малим порцијама док раствор не посветли.
У овом случају се јављају следеће реакције:
Хидроксид реагује са киселином и формира гвожђе(ИИИ) сулфат (реакција јонске измене). Он заузврат реагује са атомским водоником, који се формира током дисоцијације сумпорне киселине. Последња реакција је редокс.
Сада раствор садржи тачно сулфат који нам је потребан, али сам раствор је и даље замућен. Пустите да одстоји и филтрира, користио сам хемијски филтер.
Нерастворљиве нечистоће су остале на дну тегле:
Исперемо га и сипамо филтрирани раствор у њега. Много је лакши и чистији од оригинала.
Етил алкохол истискује соли двобазних киселина из њихових раствора. Користићемо ово својство за добијање чврстог сулфата. У раствор додамо алкохол, сипао сам 200 мл, што је по запремини једнако нешто више од половине првобитне запремине ђубрива.
На дну су се појавили кристали нашег сулфата.
Оставио сам раствор два дана тако да је сав сулфат имао времена да се исталожи.
У почетку можете додати још алкохола да бисте убрзали овај процес.
Оцедите течност, тапкањем по дну и благим загревањем, одвојите сулфат из тегле и сипајте на папирни пешкир да се осуши.
После неколико сати, сипајте сулфат у стаклену теглу, означите супстанцу и у овом облику може се чувати дуго времена.
Пошто су кристални хидрати исталожени, формула супстанце је као на слици. Али то нас не спречава да га користимо у сопствене сврхе, ионако га растварајући у води.
Закључак
Сигурносне мере и поштовање правила за руковање киселинама су дате. Ни у ком случају не смемо заборавити на њих.
Чисте супстанце свима!
Сличне мајсторске класе
Посебно занимљиво
Коментари (1)