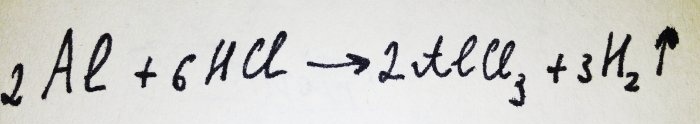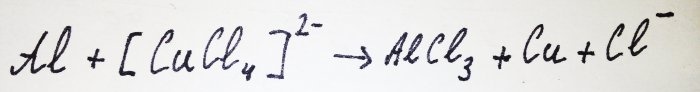Ett enkelt experiment - Blå låga
God dag, nyfikna kemister! Idag kommer vi att genomföra ett enkelt men spektakulärt experiment.
Dess väsen är att vätet som frigörs under reaktionen brinner med en blå låga.
Så vi kommer att behöva:
Vi kommer att genomföra experimentet i en glasburk.
Du kan använda en petriskål eller en bägare som kärl. Jag rekommenderar inte att använda en kolv, eftersom flödet av syre inuti kommer att vara svårt på grund av den smala halsen på kolven.
Innan du utför detta experiment rekommenderar jag starkt att du bekantar dig med säkerhetsåtgärder när du arbetar med syror.
Häll en tesked vitriol i en burk och tillsätt 40 ml syra. Lösningen blir grön på grund av bildningen av komplex kopparjontetraklorkuprat [CuCl4]2-.
Nu återstår bara att lägga till aluminiumfolien. Den är täckt med en oxidfilm, men det resulterande komplexet förstör det snabbt. Sedan reagerar en del av aluminiumet med syran, ekvationen för denna reaktion är:
Som framgår av reaktionen frigörs väte.
Resten av aluminiumet interagerar med komplexet och ersätter koppar från det:
Reaktioner sker snabbt och frigör stora mängder värme.
Vätgasen som frigörs brinner bra i luften, låt oss tända eld.
Det smala flamflödet är förknippat med egenskaperna hos burkens hals, och den rika blå färgen ges till den av kopparjoner som finns i lösningen.
Låt oss göra samma experiment, men i en annan behållare:
När allt aluminium har reagerat blir lösningen grå med fläckar av reducerad koppar på ytan. Det ska spädas med mycket vatten och hällas i avloppet.
Det finns sediment kvar längst ner:
Du bör också bli av med det, eftersom efter att ha försökt filtrera fanns en ljusbrun fällning kvar på filtret, och det kan inte kallas koppar.
Och detta avslutar denna artikel. Denna erfarenhet kan demonstreras i kemilektioner i skolan. Lycka till med din upprepning allihop!
Dess väsen är att vätet som frigörs under reaktionen brinner med en blå låga.
Reagens
Så vi kommer att behöva:
- Saltsyrakoncentration 15%;
- Kopparsulfat;
- Aluminiumfolie.
Vi kommer att genomföra experimentet i en glasburk.
Du kan använda en petriskål eller en bägare som kärl. Jag rekommenderar inte att använda en kolv, eftersom flödet av syre inuti kommer att vara svårt på grund av den smala halsen på kolven.
Experimentera
Innan du utför detta experiment rekommenderar jag starkt att du bekantar dig med säkerhetsåtgärder när du arbetar med syror.
Häll en tesked vitriol i en burk och tillsätt 40 ml syra. Lösningen blir grön på grund av bildningen av komplex kopparjontetraklorkuprat [CuCl4]2-.
Nu återstår bara att lägga till aluminiumfolien. Den är täckt med en oxidfilm, men det resulterande komplexet förstör det snabbt. Sedan reagerar en del av aluminiumet med syran, ekvationen för denna reaktion är:
Som framgår av reaktionen frigörs väte.
Resten av aluminiumet interagerar med komplexet och ersätter koppar från det:
Reaktioner sker snabbt och frigör stora mängder värme.
Vätgasen som frigörs brinner bra i luften, låt oss tända eld.
Det smala flamflödet är förknippat med egenskaperna hos burkens hals, och den rika blå färgen ges till den av kopparjoner som finns i lösningen.
Låt oss göra samma experiment, men i en annan behållare:
När allt aluminium har reagerat blir lösningen grå med fläckar av reducerad koppar på ytan. Det ska spädas med mycket vatten och hällas i avloppet.
Det finns sediment kvar längst ner:
Du bör också bli av med det, eftersom efter att ha försökt filtrera fanns en ljusbrun fällning kvar på filtret, och det kan inte kallas koppar.
Slutsats
Och detta avslutar denna artikel. Denna erfarenhet kan demonstreras i kemilektioner i skolan. Lycka till med din upprepning allihop!
Liknande mästarklasser
Särskilt intressant
Kommentarer (2)