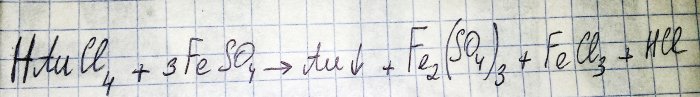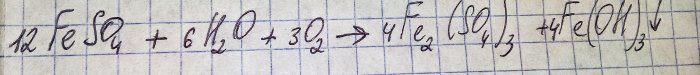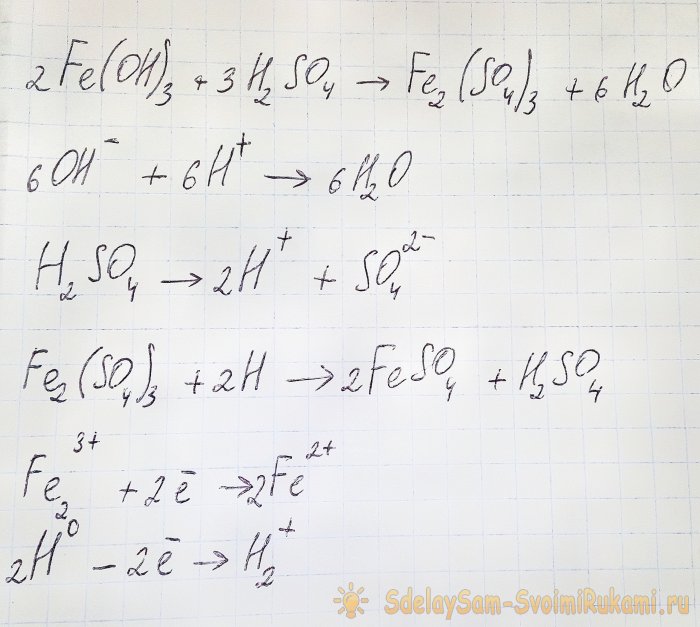Gübreden demir sülfat elde etmenin hızlı bir yolu
Radyo bileşenlerinden soy metal elde etme yolundaki sondan bir önceki adım, ikincisinin karşılık gelen klorürden indirgenmesidir. Demir(II) sülfat bu amaçlar için mükemmeldir. Bu reaksiyonun denklemini düşünün:
HAuCl4 - hidrojen tetrakloroaurat (III) - kral kral suyunda altın çözüldüğünde oluşan bir bileşik. Ayrı bir makaleyi hak ettiği için şimdilik bu sürece derinlemesine girmeyeceğiz.
Dolayısıyla sülfat (bundan sonra demir(II) sülfat kastedilmektedir) ucuz ve kolay temin edilebilen indirgeyici maddelerden biridir. Mağazalarda “demir sülfat” adı altında bulunabiliyor, gübredir. Ancak bu saf bir madde değildir, içindeki sülfat oranı yaklaşık% 50'dir, geri kalanı safsızlıktır. Altını geri kazanmadan önce sülfatımızı saflaştırmamız gerekiyor.
Gerekecek
Bunun için ihtiyacınız olacak:
- Demir sülfat (“bahçe için her şey” gibi mağazalarda satılıyor; kafama yetsin diye bir kilo aldım);
- Aküler için asit elektrolit olarak da bilinen sülfürik asit çözeltisi (otomobil bayilerinde);
- Alkolün %95'ini kullandım;
- Kimyasal veya tek kullanımlık sofra takımları (bardaklar, karıştırma kaşıkları).
Gübreden demir sülfat elde ediyoruz
Solüsyonu hazırlamak için cam kavanoz kullanıyorum. İçerisinde 500 ml sıcak su var, belki biraz daha az.
Şimdi yaklaşık yarım bardak gübreyi ölçün:
Gördüğünüz gibi, madde sarı-kahverengi renktedir, bu tür kirli "sülfat" yalnızca amaçlanan amaç için kullanılabilir - bitki örtüsünü püskürtmek için. Başka hedeflerimiz var.
Kavanozun içine dökün:
Çözelti hoş olmayan kahverengi bir renge dönüştü. Gübrenin su ile reaksiyonu sonucu oluşan renklenme:
Sülfattaki demir üç değerlikli hale oksitlenir ve aslında renginin nedeni olan demir (III) hidroksit çökelir.
Ortaya çıkan bileşiklerden ilgilendiğimiz sülfatı elde etmek için çözeltinin sülfürik asit ile asitleştirilmesi gerekir. Çözelti parlaklaşana kadar küçük porsiyonlar halinde ekleyin.
Bu durumda aşağıdaki reaksiyonlar meydana gelir:
Hidroksit asitle reaksiyona girerek demir(III) sülfat oluşturur (iyon değişim reaksiyonu). Daha sonra sülfürik asidin ayrışması sırasında oluşan atomik hidrojen ile reaksiyona girer. Son reaksiyon redokstur.
Artık çözelti tam olarak ihtiyacımız olan sülfatı içeriyor, ancak çözümün kendisi hala bulanık. Durup filtreleyin, ben kimyasal filtre kullandım.
Kavanozun dibinde çözünmeyen yabancı maddeler kaldı:
Durulayıp filtrelenen çözeltiyi içine döküyoruz. Orjinalinden çok daha hafif ve temizdir.
Etil alkol, dibazik asitlerin tuzlarını çözeltilerinden uzaklaştırır. Bu özelliği katı sülfat elde etmek için kullanacağız. Çözeltiye alkol ekliyoruz, hacim olarak gübrenin orijinal hacminin yarısından biraz fazlasına eşit olan 200 ml döktüm.
Altta sülfatımızın kristalleri belirdi.
Tüm sülfatın çökelmesine zaman kalması için çözeltiyi iki gün bıraktım.
Bu işlemi daha hızlı hale getirmek için başlangıçta daha fazla alkol ekleyebilirsiniz.
Dibine hafifçe vurarak ve hafifçe ısıtarak sıvıyı boşaltın, sülfatı kavanozdan ayırın ve kuruması için bir kağıt havlu üzerine dökün.
Birkaç saat sonra sülfatı bir cam kavanoza dökün, maddeyi etiketleyin ve bu formda uzun süre saklanabilir.
Kristal hidratlar çöktüğü için maddenin formülü resimdeki gibidir. Ancak bu, onu kendi amaçlarımız için kullanmamıza, zaten suda eritmemize engel değil.
Çözüm
Asitlerle çalışma kurallarına uyulması ve güvenlik önlemleri alınması zorunludur. Hiçbir durumda bunları unutmamalıyız.
Herkese temiz maddeler!
Benzer ana sınıflar
Özellikle ilginç
Yorumlar (1)