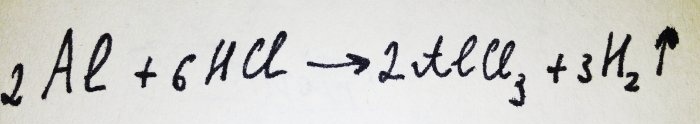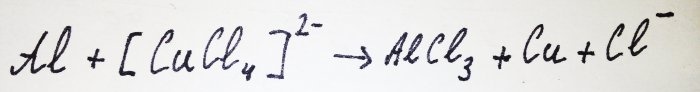Et simpelt eksperiment - Blå flamme
Goddag, nysgerrige kemikere! I dag vil vi udføre et simpelt, men spektakulært eksperiment.
Dens essens er, at den brint, der frigives under reaktionen, brænder med en blå flamme.
Så vi skal bruge:
Vi vil udføre eksperimentet i en glaskrukke.
Du kan bruge en petriskål eller et bæger som kar. Jeg anbefaler ikke at bruge en kolbe, da iltstrømmen indeni vil være vanskelig på grund af kolbens smalle hals.
Før du udfører dette eksperiment, anbefaler jeg kraftigt, at du gør dig bekendt med sikkerhedsforanstaltninger, når du arbejder med syrer.
Hæld en teskefuld vitriol i en krukke og tilsæt 40 ml syre. Opløsningen bliver grøn på grund af dannelsen af kompleks kobberion tetrachlorkuprat [CuCl4]2-.
Nu er der kun tilbage at tilføje aluminiumsfolien. Det er dækket af en oxidfilm, men det resulterende kompleks ødelægger det hurtigt. Så reagerer noget af aluminiumet med syren, ligningen for denne reaktion er:
Som det ses af reaktionen, frigives brint.
Resten af aluminiumet interagerer med komplekset og fortrænger kobber fra det:
Reaktioner opstår hurtigt og frigiver store mængder varme.
Den frigivne brint brænder godt i luften, lad os sætte ild til det.
Den smalle flammestrøm er forbundet med egenskaberne ved krukkens hals, og den rige blå farve gives til den af kobberioner, der er til stede i opløsningen.
Lad os lave det samme eksperiment, men i en anden beholder:
Når alt aluminium har reageret, bliver opløsningen grå med pletter af reduceret kobber på overfladen. Det skal fortyndes med rigeligt vand og hældes i afløbet.
Der er sediment tilbage i bunden:
Du bør også slippe af med det, da efter at have forsøgt at filtrere, forblev et lysebrunt bundfald på filteret, og det kan ikke kaldes kobber.
Og dette afslutter denne artikel. Denne erfaring kan demonstreres i kemitimerne på skolen. Held og lykke med gentagelsen alle sammen!
Dens essens er, at den brint, der frigives under reaktionen, brænder med en blå flamme.
Reagenser
Så vi skal bruge:
- Saltsyrekoncentration 15%;
- Kobbersulfat;
- Sølvpapir.
Vi vil udføre eksperimentet i en glaskrukke.
Du kan bruge en petriskål eller et bæger som kar. Jeg anbefaler ikke at bruge en kolbe, da iltstrømmen indeni vil være vanskelig på grund af kolbens smalle hals.
Eksperiment
Før du udfører dette eksperiment, anbefaler jeg kraftigt, at du gør dig bekendt med sikkerhedsforanstaltninger, når du arbejder med syrer.
Hæld en teskefuld vitriol i en krukke og tilsæt 40 ml syre. Opløsningen bliver grøn på grund af dannelsen af kompleks kobberion tetrachlorkuprat [CuCl4]2-.
Nu er der kun tilbage at tilføje aluminiumsfolien. Det er dækket af en oxidfilm, men det resulterende kompleks ødelægger det hurtigt. Så reagerer noget af aluminiumet med syren, ligningen for denne reaktion er:
Som det ses af reaktionen, frigives brint.
Resten af aluminiumet interagerer med komplekset og fortrænger kobber fra det:
Reaktioner opstår hurtigt og frigiver store mængder varme.
Den frigivne brint brænder godt i luften, lad os sætte ild til det.
Den smalle flammestrøm er forbundet med egenskaberne ved krukkens hals, og den rige blå farve gives til den af kobberioner, der er til stede i opløsningen.
Lad os lave det samme eksperiment, men i en anden beholder:
Når alt aluminium har reageret, bliver opløsningen grå med pletter af reduceret kobber på overfladen. Det skal fortyndes med rigeligt vand og hældes i afløbet.
Der er sediment tilbage i bunden:
Du bør også slippe af med det, da efter at have forsøgt at filtrere, forblev et lysebrunt bundfald på filteret, og det kan ikke kaldes kobber.
Konklusion
Og dette afslutter denne artikel. Denne erfaring kan demonstreres i kemitimerne på skolen. Held og lykke med gentagelsen alle sammen!
Lignende mesterklasser
Særlig interessant
Kommentarer (2)