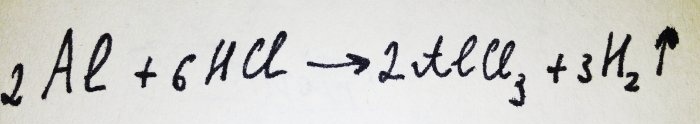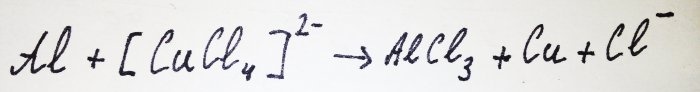Ein einfaches Experiment – Blaue Flamme
Guten Tag, neugierige Chemiker! Heute werden wir ein einfaches, aber spektakuläres Experiment durchführen.
Sein Wesen besteht darin, dass der bei der Reaktion freigesetzte Wasserstoff mit einer blauen Flamme verbrennt.
Wir benötigen also:
Wir werden das Experiment in einem Glasgefäß durchführen.
Als Gefäß können Sie eine Petrischale oder ein Becherglas verwenden. Ich empfehle nicht, eine Flasche zu verwenden, da der Sauerstofffluss ins Innere aufgrund des engen Flaschenhalses schwierig sein wird.
Ich empfehle Ihnen dringend, sich vor der Durchführung dieses Experiments mit den Sicherheitsvorkehrungen beim Umgang mit Säuren vertraut zu machen.
Gießen Sie einen Teelöffel Vitriol in ein Glas und fügen Sie 40 ml Säure hinzu. Durch die Bildung des komplexen Kupferions Tetrachlorcuprat [CuCl4]2- wird die Lösung grün.
Jetzt muss nur noch die Alufolie hinzugefügt werden. Es ist mit einem Oxidfilm bedeckt, der jedoch durch den entstehenden Komplex schnell zerstört wird. Dann reagiert ein Teil des Aluminiums mit der Säure. Die Gleichung für diese Reaktion lautet:
Wie aus der Reaktion hervorgeht, wird Wasserstoff freigesetzt.
Der Rest des Aluminiums interagiert mit dem Komplex und verdrängt Kupfer daraus:
Reaktionen laufen schnell ab und setzen große Mengen Wärme frei.
Der freigesetzte Wasserstoff brennt gut an der Luft, zünden wir ihn an.
Der schmale Flammenstrom hängt mit den Eigenschaften des Gefäßhalses zusammen, und die satte blaue Farbe wird ihm durch die in der Lösung vorhandenen Kupferionen verliehen.
Machen wir das gleiche Experiment, aber in einem anderen Container:
Wenn das gesamte Aluminium reagiert hat, wird die Lösung grau und weist Flecken reduzierten Kupfers auf der Oberfläche auf. Es sollte mit reichlich Wasser verdünnt und in den Abfluss geschüttet werden.
Am Boden sind noch Sedimente zurückgeblieben:
Sie sollten es auch entfernen, da nach dem Filterversuch ein hellbrauner Niederschlag auf dem Filter zurückblieb, der nicht als Kupfer bezeichnet werden kann.
Und damit ist dieser Artikel abgeschlossen. Diese Erfahrung lässt sich im Chemieunterricht in der Schule nachweisen. Viel Glück bei der Wiederholung euch allen!
Sein Wesen besteht darin, dass der bei der Reaktion freigesetzte Wasserstoff mit einer blauen Flamme verbrennt.
Reagenzien
Wir benötigen also:
- Salzsäurekonzentration 15 %;
- Kupfersulfat;
- Alufolie.
Wir werden das Experiment in einem Glasgefäß durchführen.
Als Gefäß können Sie eine Petrischale oder ein Becherglas verwenden. Ich empfehle nicht, eine Flasche zu verwenden, da der Sauerstofffluss ins Innere aufgrund des engen Flaschenhalses schwierig sein wird.
Experiment
Ich empfehle Ihnen dringend, sich vor der Durchführung dieses Experiments mit den Sicherheitsvorkehrungen beim Umgang mit Säuren vertraut zu machen.
Gießen Sie einen Teelöffel Vitriol in ein Glas und fügen Sie 40 ml Säure hinzu. Durch die Bildung des komplexen Kupferions Tetrachlorcuprat [CuCl4]2- wird die Lösung grün.
Jetzt muss nur noch die Alufolie hinzugefügt werden. Es ist mit einem Oxidfilm bedeckt, der jedoch durch den entstehenden Komplex schnell zerstört wird. Dann reagiert ein Teil des Aluminiums mit der Säure. Die Gleichung für diese Reaktion lautet:
Wie aus der Reaktion hervorgeht, wird Wasserstoff freigesetzt.
Der Rest des Aluminiums interagiert mit dem Komplex und verdrängt Kupfer daraus:
Reaktionen laufen schnell ab und setzen große Mengen Wärme frei.
Der freigesetzte Wasserstoff brennt gut an der Luft, zünden wir ihn an.
Der schmale Flammenstrom hängt mit den Eigenschaften des Gefäßhalses zusammen, und die satte blaue Farbe wird ihm durch die in der Lösung vorhandenen Kupferionen verliehen.
Machen wir das gleiche Experiment, aber in einem anderen Container:
Wenn das gesamte Aluminium reagiert hat, wird die Lösung grau und weist Flecken reduzierten Kupfers auf der Oberfläche auf. Es sollte mit reichlich Wasser verdünnt und in den Abfluss geschüttet werden.
Am Boden sind noch Sedimente zurückgeblieben:
Sie sollten es auch entfernen, da nach dem Filterversuch ein hellbrauner Niederschlag auf dem Filter zurückblieb, der nicht als Kupfer bezeichnet werden kann.
Abschluss
Und damit ist dieser Artikel abgeschlossen. Diese Erfahrung lässt sich im Chemieunterricht in der Schule nachweisen. Viel Glück bei der Wiederholung euch allen!
Ähnliche Meisterkurse
Besonders interessant
Kommentare (2)