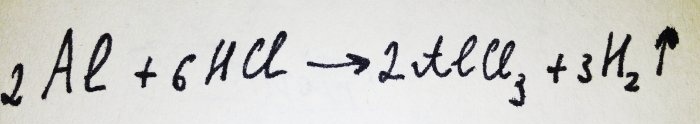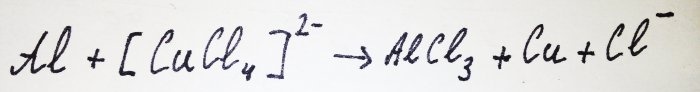Jednostavan eksperiment - Plavi plamen
Dobar dan, radoznali kemičari! Danas ćemo provesti jednostavan, ali spektakularan eksperiment.
Njegova je bit da vodik koji se oslobađa tijekom reakcije gori plavim plamenom.
Dakle, trebat će nam:
Pokus ćemo provesti u staklenoj posudi.
Kao posudu možete koristiti Petrijevu zdjelicu ili čašu. Ne preporučam korištenje tikvice jer će protok kisika unutra biti otežan zbog uskog grla tikvice.
Prije izvođenja ovog eksperimenta, toplo preporučujem da se upoznate sa sigurnosnim mjerama opreza pri radu s kiselinama.
Ulijte žličicu vitriola u staklenku i dodajte 40 ml kiseline. Otopina postaje zelena zbog stvaranja kompleksnog bakrenog iona tetraklorokuprata [CuCl4]2-.
Sada još samo preostaje dodati aluminijsku foliju. Prekriven je oksidnim filmom, ali ga nastali kompleks brzo uništava. Tada dio aluminija reagira s kiselinom, jednadžba za ovu reakciju je:
Kao što se može vidjeti iz reakcije, oslobađa se vodik.
Ostatak aluminija stupa u interakciju s kompleksom, istiskujući iz njega bakar:
Reakcije se odvijaju brzo, oslobađajući velike količine topline.
Oslobođeni vodik dobro gori na zraku, zapalimo ga.
Uzak tok plamena povezan je s karakteristikama grla staklenke, a bogatu plavu boju daju ioni bakra prisutni u otopini.
Napravimo isti eksperiment, ali u drugom spremniku:
Kad je sav aluminij reagirao, otopina postaje siva s mrljama reduciranog bakra na površini. Treba ga razrijediti s puno vode i izliti u odvod.
Ostao je talog na dnu:
Također biste se trebali riješiti toga, jer je nakon pokušaja filtriranja na filteru ostao svijetlosmeđi talog, a ne može se nazvati bakrom.
I ovime završavamo ovaj članak. Ovo iskustvo može se pokazati na satu kemije u školi. Sretno svima s ponavljanjem!
Njegova je bit da vodik koji se oslobađa tijekom reakcije gori plavim plamenom.
Reagensi
Dakle, trebat će nam:
- Koncentracija klorovodične kiseline 15%;
- Bakreni sulfat;
- Aluminijska folija.
Pokus ćemo provesti u staklenoj posudi.
Kao posudu možete koristiti Petrijevu zdjelicu ili čašu. Ne preporučam korištenje tikvice jer će protok kisika unutra biti otežan zbog uskog grla tikvice.
Eksperiment
Prije izvođenja ovog eksperimenta, toplo preporučujem da se upoznate sa sigurnosnim mjerama opreza pri radu s kiselinama.
Ulijte žličicu vitriola u staklenku i dodajte 40 ml kiseline. Otopina postaje zelena zbog stvaranja kompleksnog bakrenog iona tetraklorokuprata [CuCl4]2-.
Sada još samo preostaje dodati aluminijsku foliju. Prekriven je oksidnim filmom, ali ga nastali kompleks brzo uništava. Tada dio aluminija reagira s kiselinom, jednadžba za ovu reakciju je:
Kao što se može vidjeti iz reakcije, oslobađa se vodik.
Ostatak aluminija stupa u interakciju s kompleksom, istiskujući iz njega bakar:
Reakcije se odvijaju brzo, oslobađajući velike količine topline.
Oslobođeni vodik dobro gori na zraku, zapalimo ga.
Uzak tok plamena povezan je s karakteristikama grla staklenke, a bogatu plavu boju daju ioni bakra prisutni u otopini.
Napravimo isti eksperiment, ali u drugom spremniku:
Kad je sav aluminij reagirao, otopina postaje siva s mrljama reduciranog bakra na površini. Treba ga razrijediti s puno vode i izliti u odvod.
Ostao je talog na dnu:
Također biste se trebali riješiti toga, jer je nakon pokušaja filtriranja na filteru ostao svijetlosmeđi talog, a ne može se nazvati bakrom.
Zaključak
I ovime završavamo ovaj članak. Ovo iskustvo može se pokazati na satu kemije u školi. Sretno svima s ponavljanjem!
Slične majstorske tečajeve
Posebno zanimljivo
Komentari (2)