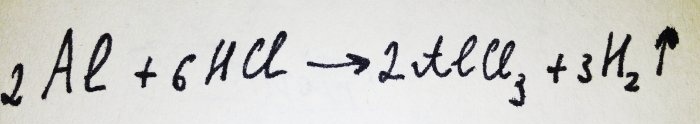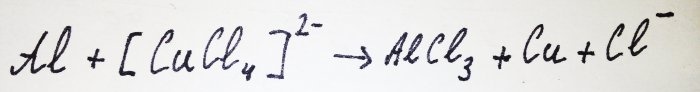Egy egyszerű kísérlet - Kék láng
Jó napot, érdeklődő vegyészek! Ma egy egyszerű, de látványos kísérletet hajtunk végre.
Lényege, hogy a reakció során felszabaduló hidrogén kék lánggal ég.
Tehát szükségünk lesz:
A kísérletet üvegedényben végezzük.
Edényként használhat Petri-csészét vagy főzőpoharat. Nem javaslom a lombik használatát, mivel a lombik keskeny nyaka miatt az oxigén áramlása nehéz lesz.
A kísérlet elvégzése előtt erősen ajánlom, hogy ismerkedjen meg a savakkal végzett munka során alkalmazott biztonsági óvintézkedésekkel.
Öntsön egy teáskanál vitriolt egy üvegbe, és adjon hozzá 40 ml savat. Az oldat zöld színűvé válik a komplex rézion-tetraklór-kuprát [CuCl4]2- képződése miatt.
Most már csak az alufólia hozzáadása van hátra. Oxidfilm borítja, de a keletkező komplex gyorsan elpusztítja. Ezután az alumínium egy része reagál a savval, ennek a reakciónak az egyenlete:
Amint a reakcióból látható, hidrogén szabadul fel.
Az alumínium többi része kölcsönhatásba lép a komplexummal, kiszorítva belőle a rezet:
A reakciók gyorsan mennek végbe, nagy mennyiségű hő szabadul fel.
A felszabaduló hidrogén jól ég a levegőben, gyújtsuk meg.
A keskeny lángfolyás az edény nyakának sajátosságaihoz kapcsolódik, a gazdag kék színt pedig az oldatban lévő rézionok adják.
Végezzük el ugyanazt a kísérletet, de egy másik tárolóban:
Amikor az összes alumínium reagált, az oldat szürkévé válik, redukált rézfoltokkal a felületén. Bő vízzel fel kell hígítani és a lefolyóba kell önteni.
Az alján üledék maradt:
Azt is meg kell szabadulni, mert a szűrés után világosbarna csapadék maradt a szűrőn, és nem nevezhető réznek.
És ezzel a cikk véget is ér. Ezt a tapasztalatot az iskolai kémiaórákon lehet bemutatni. Sok sikert mindenkinek az ismétlésedhez!
Lényege, hogy a reakció során felszabaduló hidrogén kék lánggal ég.
Reagensek
Tehát szükségünk lesz:
- Sósav koncentráció 15%;
- Rézszulfát;
- Alufólia.
A kísérletet üvegedényben végezzük.
Edényként használhat Petri-csészét vagy főzőpoharat. Nem javaslom a lombik használatát, mivel a lombik keskeny nyaka miatt az oxigén áramlása nehéz lesz.
Kísérlet
A kísérlet elvégzése előtt erősen ajánlom, hogy ismerkedjen meg a savakkal végzett munka során alkalmazott biztonsági óvintézkedésekkel.
Öntsön egy teáskanál vitriolt egy üvegbe, és adjon hozzá 40 ml savat. Az oldat zöld színűvé válik a komplex rézion-tetraklór-kuprát [CuCl4]2- képződése miatt.
Most már csak az alufólia hozzáadása van hátra. Oxidfilm borítja, de a keletkező komplex gyorsan elpusztítja. Ezután az alumínium egy része reagál a savval, ennek a reakciónak az egyenlete:
Amint a reakcióból látható, hidrogén szabadul fel.
Az alumínium többi része kölcsönhatásba lép a komplexummal, kiszorítva belőle a rezet:
A reakciók gyorsan mennek végbe, nagy mennyiségű hő szabadul fel.
A felszabaduló hidrogén jól ég a levegőben, gyújtsuk meg.
A keskeny lángfolyás az edény nyakának sajátosságaihoz kapcsolódik, a gazdag kék színt pedig az oldatban lévő rézionok adják.
Végezzük el ugyanazt a kísérletet, de egy másik tárolóban:
Amikor az összes alumínium reagált, az oldat szürkévé válik, redukált rézfoltokkal a felületén. Bő vízzel fel kell hígítani és a lefolyóba kell önteni.
Az alján üledék maradt:
Azt is meg kell szabadulni, mert a szűrés után világosbarna csapadék maradt a szűrőn, és nem nevezhető réznek.
Következtetés
És ezzel a cikk véget is ér. Ezt a tapasztalatot az iskolai kémiaórákon lehet bemutatni. Sok sikert mindenkinek az ismétlésedhez!
Hasonló mesterkurzusok
Különösen érdekes
Megjegyzések (2)