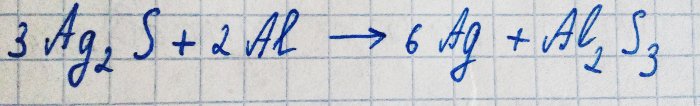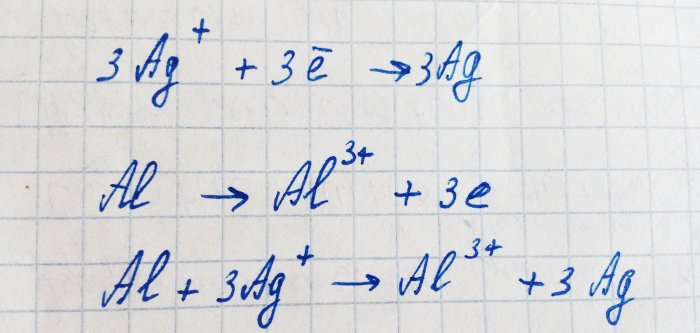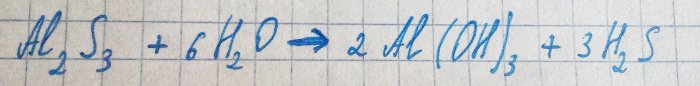Zilveren voorwerpen thuis schoonmaken
Onlangs kwam ik een zilveren bestekset tegen van ongeveer honderd jaar oud. Gedurende deze tijd slaagden de lepels en messen erin donker te worden en te roesten, en ik besloot ze te verwijderen van de afzettingen die zich hadden gevormd. In dit artikel deel ik een redelijk effectieve manier om je antieke bestek weer in zijn oorspronkelijke glans te brengen. Dus laten we gaan.
Theorie
Laten we eerst eens kijken waarom zilver na verloop van tijd donkerder wordt en waar roest vandaan komt.
Zilver (Ag) vertoont vrijwel geen reactiviteit met zuurstof of water, dat wil zeggen dat het niet roest. Deze eigenschap werd voor het eerst opgemerkt door alchemisten; ze begonnen zilver een edelmetaal te noemen.
Zilver reageert echter met waterstofsulfide in aanwezigheid van zuurstof. De vergelijking voor deze reactie is als volgt:
Het resulterende zilversulfide bedekt het metaal slechts met een donkere film, waardoor verdere oxidatie wordt voorkomen.
Als het bestek niet van puur zilver is gemaakt (bijvoorbeeld standaard 800), dan roesten onzuiverheden in de legering.
Roest verwijderen
Bereid een oplossing van citroenzuur. Hoe meer verzadigd het is, hoe sneller en gewelddadiger de reactie zal verlopen.We stoppen er bestek in, als er geen gasbellen meer vrijkomen, halen we ze uit de oplossing, spoelen ze af met water en vegen ze af met keukenpapier.
Voor het beste resultaat kunt u de oplossing tot 80°C verwarmen, maar het is belangrijk dat u de veiligheidsmaatregelen in acht neemt.
Verwijdering van tandplak
Om tandplak te verwijderen, gebruiken we de chemische methode om zilversulfide te reduceren tot vrij metaal.
Hiervoor hebben we nodig:
- - de container waarin de reactie zal plaatsvinden;
- - natriumcarbonaat;
- - aluminiumfolie;
- - tafel zout;
- - heet water.
Plaats aluminiumfolie op de bodem van het vat en zilveren voorwerpen erop, met de donkere kant naar beneden.
Strooi er frisdrank overheen.
Los nu het zout op in water met een snelheid van 6 eetlepels per liter water. Giet de resulterende oplossing in de container, een reactie begint met het vrijkomen van waterstofsulfide en koolstofdioxide.
Het hele proces moet buiten worden uitgevoerd, omdat waterstofsulfide een karakteristieke geur van rotte eieren heeft en schadelijk is voor de gezondheid.
Laten we eens kijken naar de chemie van wat er gebeurt.
Eerst lost de soda de dunne hydroxidefilm op van het oppervlak van de folie.
Hierdoor krijgt het zilversulfide de kans direct te reageren met het aluminium.
Aluminium heeft een lagere ionisatie-energie dan zilver. Het oxideert tot een ion, waardoor zilver zijn elektronen krijgt. Dit proces kan als volgt worden geschreven:
Deze reactie is elektrochemisch: door de beweging van elektronen van aluminium naar zilver ontstaat er een potentiaalverschil.
Zout in een oplossing verbetert de geleidbaarheid ervan, waardoor de reactie volledig kan verlopen.
Het vrijkomende aluminiumsulfide reageert onmiddellijk met water:
Vandaar het waterstofsulfide en de bijbehorende geur.
Dit proces kan maximaal een half uur duren. Als u klaar bent, spoelt u het bestek af met water en droogt u het af met een handdoek.
Na zilverrestauratie kunt u speciale middelen gebruiken om het te conserveren. Ze beschermen het zilveroppervlak tegen vocht en waterstofsulfide.
Hierdoor zal het zilver lang zijn glans behouden.
Conclusie
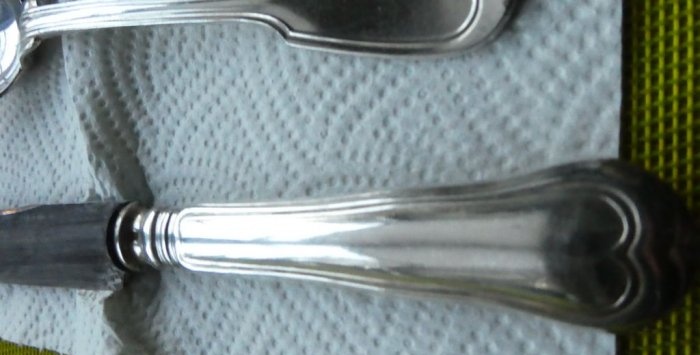
Foto's van gerestaureerde gerechten:
Zoals je kunt zien, is er geen spoor van verdonkering op de lepels te zien. De messen begonnen er ook beter uit te zien, maar helaas verdween een deel van de zilverlaag van het oppervlak; de tijd eist nog steeds zijn tol. Je moet ze naar een specialist brengen om ze opnieuw te verzilveren.
En dit artikel is ten einde. Veel succes met jullie herhaling allemaal!
Origineel artikel in het Engels
Soortgelijke masterclasses
Bijzonder interessant
Opmerkingen (0)