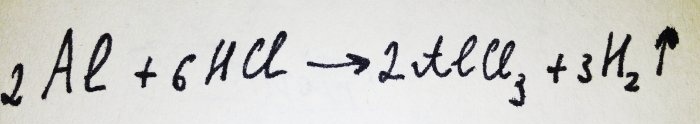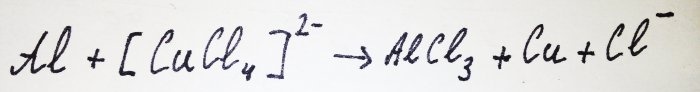Et enkelt eksperiment - Blå flamme
God dag, nysgjerrige kjemikere! I dag skal vi gjennomføre et enkelt, men spektakulært eksperiment.
Dens essens er at hydrogenet som frigjøres under reaksjonen brenner med en blå flamme.
Så vi trenger:
Vi skal gjennomføre forsøket i en glasskrukke.
Du kan bruke en petriskål eller et beger som kar. Jeg anbefaler ikke å bruke en kolbe, siden strømmen av oksygen inni vil være vanskelig på grunn av den smale halsen på kolben.
Før du utfører dette eksperimentet, anbefaler jeg på det sterkeste at du gjør deg kjent med sikkerhetstiltak når du arbeider med syrer.
Hell en teskje vitriol i en krukke og tilsett 40 ml syre. Løsningen blir grønn på grunn av dannelsen av kompleks kobberion tetraklorkuprat [CuCl4]2-.
Nå gjenstår det bare å legge til aluminiumsfolien. Den er dekket med en oksidfilm, men det resulterende komplekset ødelegger det raskt. Deretter reagerer noe av aluminiumet med syren, ligningen for denne reaksjonen er:
Som det fremgår av reaksjonen, frigjøres hydrogen.
Resten av aluminiumet samhandler med komplekset og fortrenger kobber fra det:
Reaksjoner skjer raskt, og frigjør store mengder varme.
Hydrogenet som frigjøres brenner godt i luft, la oss sette fyr på det.
Den smale flammestrømmen er assosiert med egenskapene til krukkens hals, og den rike blå fargen er gitt til den av kobberioner som er tilstede i løsningen.
La oss gjøre det samme eksperimentet, men i en annen beholder:
Når alt aluminiumet har reagert, blir løsningen grå med flekker av redusert kobber på overflaten. Den skal fortynnes med mye vann og helles i avløpet.
Det er sediment igjen nederst:
Du bør også kvitte deg med det, siden etter å ha prøvd å filtrere, forble et lysebrunt bunnfall på filteret, og det kan ikke kalles kobber.
Og dette avslutter denne artikkelen. Denne erfaringen kan demonstreres i kjemitimer på skolen. Lykke til med repetisjonen alle sammen!
Dens essens er at hydrogenet som frigjøres under reaksjonen brenner med en blå flamme.
Reagenser
Så vi trenger:
- Saltsyrekonsentrasjon 15 %;
- Kobbersulfat;
- Aluminiumsfolie.
Vi skal gjennomføre forsøket i en glasskrukke.
Du kan bruke en petriskål eller et beger som kar. Jeg anbefaler ikke å bruke en kolbe, siden strømmen av oksygen inni vil være vanskelig på grunn av den smale halsen på kolben.
Eksperiment
Før du utfører dette eksperimentet, anbefaler jeg på det sterkeste at du gjør deg kjent med sikkerhetstiltak når du arbeider med syrer.
Hell en teskje vitriol i en krukke og tilsett 40 ml syre. Løsningen blir grønn på grunn av dannelsen av kompleks kobberion tetraklorkuprat [CuCl4]2-.
Nå gjenstår det bare å legge til aluminiumsfolien. Den er dekket med en oksidfilm, men det resulterende komplekset ødelegger det raskt. Deretter reagerer noe av aluminiumet med syren, ligningen for denne reaksjonen er:
Som det fremgår av reaksjonen, frigjøres hydrogen.
Resten av aluminiumet samhandler med komplekset og fortrenger kobber fra det:
Reaksjoner skjer raskt, og frigjør store mengder varme.
Hydrogenet som frigjøres brenner godt i luft, la oss sette fyr på det.
Den smale flammestrømmen er assosiert med egenskapene til krukkens hals, og den rike blå fargen er gitt til den av kobberioner som er tilstede i løsningen.
La oss gjøre det samme eksperimentet, men i en annen beholder:
Når alt aluminiumet har reagert, blir løsningen grå med flekker av redusert kobber på overflaten. Den skal fortynnes med mye vann og helles i avløpet.
Det er sediment igjen nederst:
Du bør også kvitte deg med det, siden etter å ha prøvd å filtrere, forble et lysebrunt bunnfall på filteret, og det kan ikke kalles kobber.
Konklusjon
Og dette avslutter denne artikkelen. Denne erfaringen kan demonstreres i kjemitimer på skolen. Lykke til med repetisjonen alle sammen!
Lignende mesterklasser
Spesielt interessant
Kommentarer (2)