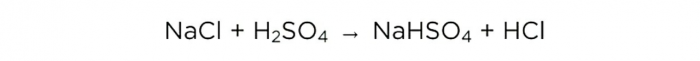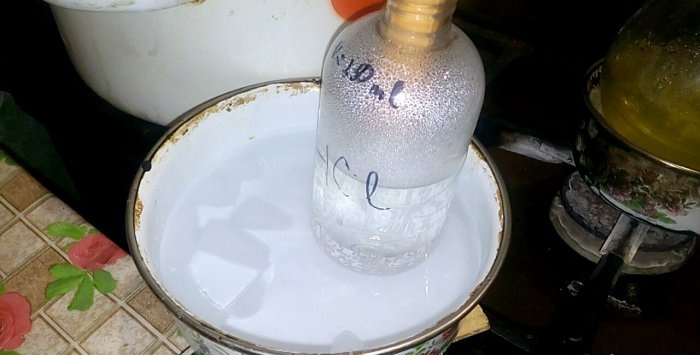Wytwarzanie kwasu solnego w domu
Alchemicy, którzy jako pierwsi wyprodukowali kwas solny w XV wieku, nazywali go „spiritus salis”, „spirytusem z soli”. Kwas ten miał wówczas magiczne właściwości: powodował korozję papieru, rozpuszczał metale i zatruwał ludzi. Te właściwości pozostały z nim do dziś, ale teraz ten kwas został wystarczająco zbadany i nie ma tu żadnej magii.
Kwas solny (HCl) jest mocnym kwasem jednozasadowym, w czystej postaci jest przezroczystą cieczą. Przy maksymalnym stężeniu 38% „dymi” w powietrzu. Otrzymamy kwas o stężeniu o połowę mniejszym.
Więc zacznijmy.
Środki ostrożności
Zachowaj ostrożność podczas pracy z substancjami toksycznymi!
Wszystkie doświadczenia należy przeprowadzać w dobrze wentylowanym pomieszczeniu lub pod kapturem.Załóż okulary ochronne (można je kupić w sklepie z narzędziami) i rękawiczki (jeśli nie możesz znaleźć specjalnych rękawic chemicznych, odpowiednie będą dobrej jakości) do mycia naczyń).
Soda oczyszczona musi być obecna na miejscu doświadczenia, aby w nieprzewidzianej sytuacji zneutralizować kwas (powoduje to uwolnienie dwutlenku węgla i wody).
Surowo zabrania się przeprowadzania eksperymentów w pojemnikach metalowych.
Będzie potrzebował
Do przeprowadzenia doświadczenia będziemy potrzebować:
- Kwaśny elektrolit do akumulatorów (sprzedawany w sklepie samochodowym);
- Woda destylowana (ibid);
- Sól kuchenna (dostępna w każdej kuchni);
- Soda oczyszczona (patrz środki bezpieczeństwa).
Z naczyń, których potrzebujesz:
- Kolba szklana;
- Naczynie z piaskiem, w którym można umieścić kolbę;
- Kilka jednorazowych kubków 200 ml;
Jeśli masz żaroodporną kolbę, możesz ją podgrzać pod otwartym płomieniem palnika. Ale nadal zalecam używanie piasku, w którym to przypadku wchłonie kwas.
Przyda Ci się także para kątowników hydraulicznych o średnicy 50 mm i palnik (w moim przypadku alkoholowy, ale ja polecam gazowy).
Etap 1 - parowanie
Elektrolitem do akumulatorów jest 36% kwas siarkowy (H2SO4). Najpierw musimy zwiększyć jego stężenie.
Do szklanki wlać 200 ml, czyli prawie po brzegi i wlać do kolby nieco więcej niż połowę szklanki. Zaznacz markerem i dodaj resztę.
Dla bardziej wydajnego ogrzewania umieściłem reflektor foliowy wokół kolby, ale później go usunąłem, ponieważ zaczął się topić.
Teraz postaw kolbę na palniku i odparuj do poziomu wcześniej ustawionego znaku, a nawet trochę niżej.
Jednocześnie na róg kładziemy kilkukrotnie złożoną gazę i zabezpieczamy gumką. Przygotuj nienasycony roztwór sody i zanurz w nim koniec rogu gazą.
Kiedy elektrolit zaczyna wrzeć, kładziemy róg na kolbie, mocno na niej przylega. Kierujemy koniec gazy do otwartego okna.
Jest to konieczne, jeśli nagle sam kwas siarkowy zacznie parować wraz z wodą. Jeśli nie przegrzejesz kolby zbyt mocno, nic takiego się nie stanie.
Palnik w akcji:
Mój palnik ma stosunkowo małą moc, więc odparowywanie trwało około godziny.Palnik gazowy lub kuchenka elektryczna znacznie przyspieszy ten proces.
Po zakończeniu pierwszego etapu w kolbie powinna pozostać nieco mniej niż połowa roztworu, czyli kwas o stężeniu około 75%. Nie zapomnij o dokładności.
Pozostawić do ostygnięcia do temperatury pokojowej.
Etap 2 – obliczenia
Teraz, gdy mamy stężony kwas siarkowy, możemy przeprowadzić reakcję zasadową, która wygląda następująco:
Ale najpierw wykonajmy obliczenia, a na koniec porównamy je z tym, co wydarzyło się w praktyce.
Tak więc początkowo mieliśmy 200ml elektrolitu o gęstości 1,27 g/cm3. Patrząc na tabelę gęstości kwasu siarkowego, widzimy, że gęstość ta odpowiada stężeniu 36%. Obliczmy objętość kwasu:
200ml*36%=72ml - V(H2SO4)
Po odparowaniu roztworu jego stężenie, a co za tym idzie i gęstość, wzrosło. Patrzymy na tę samą tabelę i widzimy, że stężenie 75% odpowiada gęstości 1,67 g/cm3.
Znając aktualną gęstość (p) i objętość (V) kwasu, dowiadujemy się o masie:
m=p*V;
m(H2SO4)=1,67g/cm3 * 72ml=120g;
m(H2SO4)=1,67g/cm3 * 72ml=120g;
Teraz pamiętamy z chemii szkolnej:
m(H2SO4)/M(H2SO4)=m(NaCl)/M(NaCl)=m(HCl)/M(HCl),
gdzie M jest masą molową substancji.
gdzie M jest masą molową substancji.
Masy molowe H2SO4, NaCl i HCl wynoszą odpowiednio 98, 58,5 i 36,5 g/mol. Teraz możemy dowiedzieć się, ile soli kuchennej potrzeba i ile HCl otrzymamy.
Mianowicie potrzebujemy 72 g NaCl, czyli 34 ml, weźmy go w nadmiarze – ćwierć szklanki.
Świetnie, a HCl w teorii wyjdzie na 44,7 g.
Tabela gęstości HCl zawiera kolumnę g/l. Bierzemy stąd wartość dla stężenia 15% – 166,4 g/l. Objętość wody potrzebna do uzyskania 15% HCl wynosi 44,7/166,4≈270ml. Weźmiemy 200 ml. W rezultacie teoretycznie otrzymam 22% kwas solny.
Etap 3 – uzyskanie kwasu
Łączymy dwa rogi w następujący sposób:
A cała konstrukcja będzie wyglądać następująco:
Odpowiedni kwas skondensuje się w naczyniu oznaczonym HCl; objętość zawartej w nim wody wynosi 200 ml. Zaznacz także aktualny poziom cieczy na tym pojemniku.
Usuwamy rogi i wlewamy obliczoną ilość soli do kolby przez lejek.
Roztwór zmienia kolor na żółty.
Aby kwas solny zaczął się uwalniać, należy włączyć palnik. Ale najpierw szczelnie mocujemy rogi do kolby i naczynia odbiorczego.
Kiedy kwas skrapla się w wodzie, powstają „fale pionowe”. Ponadto roztwór nagrzewa się i musi zostać schłodzony. Na przykład możesz umieścić pod spodem kolejne naczynie z lodem.
Reakcja przebiega stosunkowo szybko - 20 minut, po czym można wyłączyć ogrzewanie. Pozwól, aby ostatnie pary kwasu solnego rozpuściły się w wodzie, a następnie szczelnie zamknij naczynie. Po ostygnięciu kolby pozostały roztwór rozcieńczyć wodą (w przybliżeniu jeden do jednego) i wlać do kanalizacji.
Konkluzja
Po znaku na naczyniu określamy, ile płynu zostało dodanego. U mnie jest to ⅙, czyli 17%. To jest stężenie naszego kwasu solnego. Porównajmy to z uzyskanym w teorii.
17%/22%*100%=77% - wydajność reakcji.
Należy zauważyć, że nie ma wyjścia równego 1, zawsze są straty. W moim przypadku jest to niedostatecznie odparowany elektrolit. Idealnie stężenie kwasu siarkowego powinno wynosić 90-95%.
Sprawdźmy powstały kwas pod kątem interakcji z metalem.
Obserwujemy szybką ewolucję wodoru. Oznacza to, że kwas nadaje się do dalszych eksperymentów.
Wariacje
Jako kolbę możesz użyć czystej szklanej butelki po piwie lub napoju gazowanym, ale pod warunkiem, że ogrzewanie będzie możliwie płynne. Zamiast narożników PCV można wziąć rurki i narożniki polipropylenowe o mniejszej średnicy (odpowiedniej dla Twojej kolby).
Jeszcze raz apeluję o zachowanie środków ostrożności. Życzę wszystkim miłych przeżyć!
Podobne klasy mistrzowskie
Szczególnie interesujące
Komentarze (19)