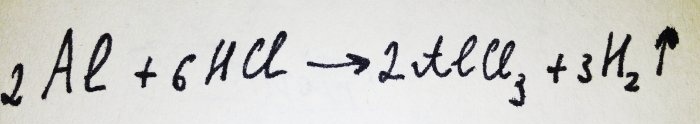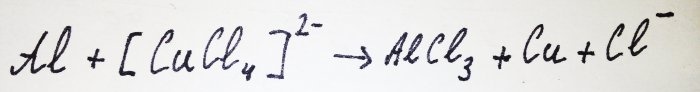Uma experiência simples - Chama Azul
Bom dia, químicos curiosos! Hoje realizaremos um experimento simples, mas espetacular.
Sua essência é que o hidrogênio liberado durante a reação queime com uma chama azul.
Então, precisaremos de:
Faremos o experimento em uma jarra de vidro.
Você pode usar uma placa de Petri ou um copo como recipiente. Não recomendo o uso de frasco, pois o fluxo de oxigênio em seu interior será difícil devido ao gargalo estreito do frasco.
Antes de realizar este experimento, recomendo fortemente que você se familiarize com as precauções de segurança ao trabalhar com ácidos.
Despeje uma colher de chá de vitríolo em uma jarra e adicione 40 ml de ácido. A solução fica verde devido à formação do complexo tetraclorocuprato de íon cobre [CuCl4]2-.
Agora só falta adicionar o papel alumínio. É coberto por uma película de óxido, mas o complexo resultante o destrói rapidamente. Então parte do alumínio reage com o ácido, a equação para esta reação é:
Como pode ser visto na reação, o hidrogênio é liberado.
O resto do alumínio interage com o complexo, deslocando o cobre dele:
As reações ocorrem rapidamente, liberando grandes quantidades de calor.
O hidrogênio liberado queima bem no ar, vamos atear fogo.
O estreito fluxo da chama está associado às características do gargalo da jarra, e a rica cor azul lhe é dada pelos íons de cobre presentes na solução.
Vamos fazer o mesmo experimento, mas em um contêiner diferente:
Quando todo o alumínio tiver reagido, a solução ficará cinza com manchas de cobre reduzido na superfície. Deve ser diluído em bastante água e despejado no ralo.
Há sedimentos deixados no fundo:
Você também deve se livrar dele, pois depois de tentar filtrar ficou um precipitado marrom claro no filtro, que não pode ser chamado de cobre.
E isso conclui este artigo. Essa experiência pode ser demonstrada nas aulas de química na escola. Boa sorte com sua repetição a todos!
Sua essência é que o hidrogênio liberado durante a reação queime com uma chama azul.
Reagentes
Então, precisaremos de:
- Concentração de ácido clorídrico 15%;
- Sulfato de cobre;
- Folha de alumínio.
Faremos o experimento em uma jarra de vidro.
Você pode usar uma placa de Petri ou um copo como recipiente. Não recomendo o uso de frasco, pois o fluxo de oxigênio em seu interior será difícil devido ao gargalo estreito do frasco.
Experimentar
Antes de realizar este experimento, recomendo fortemente que você se familiarize com as precauções de segurança ao trabalhar com ácidos.
Despeje uma colher de chá de vitríolo em uma jarra e adicione 40 ml de ácido. A solução fica verde devido à formação do complexo tetraclorocuprato de íon cobre [CuCl4]2-.
Agora só falta adicionar o papel alumínio. É coberto por uma película de óxido, mas o complexo resultante o destrói rapidamente. Então parte do alumínio reage com o ácido, a equação para esta reação é:
Como pode ser visto na reação, o hidrogênio é liberado.
O resto do alumínio interage com o complexo, deslocando o cobre dele:
As reações ocorrem rapidamente, liberando grandes quantidades de calor.
O hidrogênio liberado queima bem no ar, vamos atear fogo.
O estreito fluxo da chama está associado às características do gargalo da jarra, e a rica cor azul lhe é dada pelos íons de cobre presentes na solução.
Vamos fazer o mesmo experimento, mas em um contêiner diferente:
Quando todo o alumínio tiver reagido, a solução ficará cinza com manchas de cobre reduzido na superfície. Deve ser diluído em bastante água e despejado no ralo.
Há sedimentos deixados no fundo:
Você também deve se livrar dele, pois depois de tentar filtrar ficou um precipitado marrom claro no filtro, que não pode ser chamado de cobre.
Conclusão
E isso conclui este artigo. Essa experiência pode ser demonstrada nas aulas de química na escola. Boa sorte com sua repetição a todos!
Master classes semelhantes
Particularmente interessante
Comentários (2)