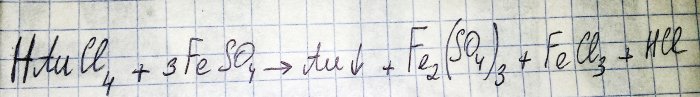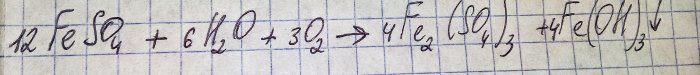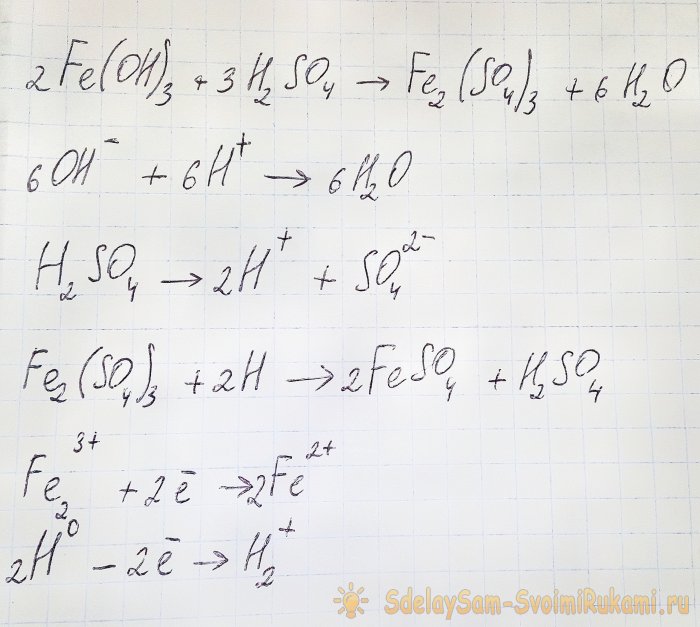Isang mabilis na paraan upang makakuha ng ferrous sulfate mula sa pataba
Ang penultimate na hakbang sa landas sa pagkuha ng isang marangal na metal mula sa mga bahagi ng radyo ay ang pagbawas ng huli mula sa kaukulang klorido. Ang iron(II) sulfate ay mahusay para sa mga layuning ito. Isaalang-alang ang equation para sa reaksyong ito:
HAuCl4 - hydrogen tetrachloroaurate (III) - isang tambalang nabubuo kapag ang ginto ay natunaw sa aqua regia. Hindi na kami lalalim sa prosesong ito sa ngayon, dahil nararapat ito sa isang hiwalay na artikulo.
Kaya, ang sulfate (pagkatapos nito ay iron(II) sulfate ay sinadya) ay isa sa mura at madaling magagamit na mga ahente ng pagbabawas. Sa mga tindahan maaari itong matagpuan sa ilalim ng pangalang "iron sulfate", ito ay isang pataba. Ngunit ito ay hindi isang purong sangkap, ang proporsyon ng sulpate sa loob nito ay halos 50%, ang natitira ay mga impurities. At bago natin maibalik ang ginto, kailangan nating linisin ang ating sulfate.
Kakailanganin
Para dito kakailanganin mo:
- Iron sulfate (ibinebenta sa mga tindahan tulad ng "lahat para sa hardin"; bumili ako ng isang kilo upang magkaroon ako ng sapat para sa aking ulo);
- Sulfuric acid solution, kilala rin bilang acid electrolyte para sa mga baterya (sa mga dealership ng kotse);
- Alkohol, gumamit ako ng 95%;
- Kemikal o disposable tableware (mga tasa, stirring spoons).
Kumuha kami ng iron sulfate mula sa pataba
Gumagamit ako ng garapon ng salamin upang ihanda ang solusyon. Sa loob mayroong 500 ML ng mainit na tubig, marahil ay mas kaunti.
Ngayon sukatin ang halos kalahating baso ng pataba:
Tulad ng nakikita mo, ang sangkap ay dilaw-kayumanggi sa kulay; ang gayong maruming "sulpate" ay maaari lamang gamitin para sa nilalayon nitong layunin - upang mag-spray ng mga halaman. Mayroon kaming iba pang mga layunin.
Ibuhos ito sa garapon:
Ang solusyon ay naging isang hindi kasiya-siyang kayumanggi na kulay. Ang pangkulay ay naganap dahil sa reaksyon ng pataba sa tubig:
Ang iron sa sulfate ay na-oxidized sa trivalent, at ang iron(III) hydroxide ay namuo, na talagang dahilan ng kulay nito.
Upang makuha ang sulpate na interesado kami mula sa mga nagresultang compound, kinakailangan na i-acidify ang solusyon na may sulfuric acid. Magdagdag ng maliliit na bahagi hanggang sa lumiwanag ang solusyon.
Sa kasong ito, nangyayari ang mga sumusunod na reaksyon:
Ang hydroxide ay tumutugon sa acid upang bumuo ng iron(III) sulfate (ion exchange reaction). Ito naman ay tumutugon sa atomic hydrogen, na nabuo sa panahon ng dissociation ng sulfuric acid. Ang huling reaksyon ay redox.
Ngayon ang solusyon ay naglalaman ng eksaktong sulpate na kailangan namin, ngunit ang solusyon mismo ay maulap pa rin. Hayaang umupo at salain, gumamit ako ng chemical filter.
Ang mga hindi matutunaw na dumi ay nanatili sa ilalim ng garapon:
Banlawan namin ito at ibuhos ang na-filter na solusyon dito. Ito ay mas magaan at mas malinis kaysa sa orihinal.
Ang ethyl alcohol ay nag-aalis ng mga asin ng mga dibasic acid mula sa kanilang mga solusyon. Gagamitin namin ang property na ito para makakuha ng solid sulfate. Nagdagdag kami ng alkohol sa solusyon, nagbuhos ako ng 200 ML, na katumbas ng dami ng higit sa kalahati ng orihinal na dami ng pataba.
Ang mga kristal ng aming sulfate ay lumitaw sa ibaba.
Iniwan ko ang solusyon sa loob ng dalawang araw upang ang lahat ng sulpate ay may oras na umuna.
Maaari kang magdagdag ng alkohol sa simula upang mapabilis ang prosesong ito.
Alisan ng tubig ang likido, gamit ang pagtapik sa ibaba at banayad na pagpainit, paghiwalayin ang sulfate mula sa garapon at ibuhos ito sa isang tuwalya ng papel upang matuyo.
Pagkatapos ng ilang oras, ibuhos ang sulpate sa isang garapon ng salamin, lagyan ng label ang sangkap, at sa form na ito maaari itong maimbak nang mahabang panahon.
Dahil ang mga crystalline hydrates ay namuo, ang formula ng sangkap ay tulad ng nasa larawan. Ngunit hindi ito pumipigil sa amin na gamitin ito para sa aming sariling mga layunin, na dissolving ito sa tubig pa rin.
Konklusyon
Ang mga pag-iingat sa kaligtasan at pagsunod sa mga patakaran para sa paghawak ng mga acid ay ibinigay. Sa anumang pagkakataon ay hindi natin dapat kalimutan ang tungkol sa kanila.
Malinis na mga sangkap sa lahat!
Mga katulad na master class
Lalo na kawili-wili
Mga komento (1)